¿Pasar de líquido a sólido?
Solidificación. Al restar calor se logra la solidificación, es decir, la transformación de líquido a sólido. Dado que este es el proceso inverso al de fusión, es fácil deducir que la temperatura que determina la solidificación es la misma que determina la transición de sólido a líquido.
¿Cómo se llama el paso de sólido a líquido?
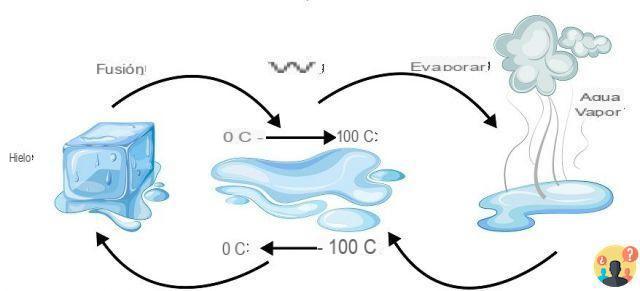
Fusión: la transición del estado sólido al líquido; Evaporación: la transición del estado líquido al gaseoso; en el ciclo del agua ocurre cuando el agua de los mares, lagos y ríos calentados por el sol se evapora y asciende hacia el cielo.
¿Cuándo un vapor se vuelve sólido?
La condensación o escarcha es el paso directo de un material del estado gaseoso al estado sólido (como la formación de escarcha).
¿Cómo se producen los cambios de estado?
Cuando un cuerpo se calienta, la energía de las partículas aumenta hasta vencer a las fuerzas cohesivas, provocando la transición de estado; al contrario, al enfriarlo, las partículas disminuyen su movimiento y se sienten más las fuerzas de cohesión.
¿Cómo se llama la transición de gas a sólido?
escarcha: paso del estado gaseoso al sólido (exotérmico);
Sólidos, líquidos y gases: los estados físicos de la materia
Encuentra 22 preguntas relacionadas
¿Cuáles son los 6 cambios de estado?
la transición del estado sólido al líquido → fusión. transición de estado líquido a gaseoso → vaporización. transición de estado gaseoso a líquido → condensación. la transición del estado sólido al gaseoso → sublimación.
¿Cómo se define la temperatura a la que coexisten las fases sólida y líquida?
El punto de fusión y la temperatura de fusión
El punto de fusión de una sustancia se define como el valor de temperatura y presión en el que las fases sólida y líquida coexisten en equilibrio termodinámico, es decir, sin que exista una transición entre las dos fases.
¿Cómo identificas las temperaturas de los cambios de estado?
Procedimiento: ante todo es necesario darse cuenta que de -20°C a 130°C hay dos cambios de estado: - el primero a 0°C (fusión), en el que el hielo se convierte en agua líquida; - la segunda a 100°C (evaporación), en la que el agua líquida se convierte en vapor de agua.
¿Cuáles son los cambios en el estado del agua?
Evaporación: la transición del estado líquido al gaseoso; Condensación: la transición del estado gaseoso al líquido; Congelación: la transición del estado líquido al sólido; Sublimación: el paso del estado sólido al gaseoso.
¿Cómo se lleva a cabo la solidificación del agua?
El agua proporciona el ejemplo más claro de solidificación. Cuando el agua líquida se enfría hasta que alcanza su temperatura de fusión, comienza a solidificarse y sus moléculas comienzan a ordenarse, formando la red cristalina de hielo.
¿A qué se debe el fenómeno Frost?
Para que se produzca la helada es necesario que existan condiciones de temperatura pero también de presión, ad hoc, en el entorno. De lo contrario, el cambio de estado se realiza en varias etapas "según lo programado". La temperatura es, por tanto, un factor importante, a tener en cuenta, en el estudio de este proceso, pero no es el único.
¿Qué cambios de estado requieren energía?
Evaporación: transición de líquido a gaseoso. Condensación: transición de gaseoso a líquido. Solidificación: transición de líquido a sólido. Sublimación: transición directa de sólido a gaseoso.
¿Cómo afecta la presión sobre los cambios de estado?
En cuanto a la presión, actúa de forma inversa a la temperatura: un aumento de presión favorece los pasos del estado gaseoso al estado líquido o del estado líquido al estado sólido, mientras que su disminución favorece los pasos inversos.
¿Por qué los líquidos pueden cambiar de forma sin cambiar de volumen?
Las moléculas de un líquido están en continuo movimiento recíproco y, a diferencia de lo que ocurre en un gas, se deslizan unas sobre otras sin separarse. Es por ello que los líquidos tienen volumen propio, toman la forma del recipiente que los contiene y son prácticamente incompresibles.
¿Cuáles son los cambios de estado para el enfriamiento?
Al calentar una sustancia pasa del estado sólido al líquido o gaseoso (gaseosa), al contrario al enfriarse se producen los procesos inversos: condensación y solidificación.
¿Por qué el agua cambia de estado?
El cambio de temperatura provoca el cambio en el estado del agua. Cuando la temperatura baja mucho, el agua cambia de estado líquido a sólido, convirtiéndose en hielo. ... Cuando el vapor de agua se enfría, se condensa y regresa en forma de agua en estado líquido.
¿Cuáles son los cambios en el estado del agua que determinan las nevadas?
En el interior de una nube coexiste la presencia de agua en estado sólido, líquido y gaseoso; el equilibrio de estas tres fases está controlado por la temperatura y la presión y determina la forma del cristal de nieve.
¿Cómo son los enlaces entre las moléculas de un líquido?
En estado líquido, las partículas, aunque se mueven libremente, están sujetas a fuerzas de atracción electrostática mutua y, a menudo, también a interacciones intermoleculares (enlaces entre moléculas) que son bastante fuertes y tienden a organizarse en capas superpuestas, adaptándose a la forma del recipiente que los contiene. .
¿Por qué la temperatura permanece constante durante los cambios de estado?
Aunque continúa calentándose, durante todo el cambio de estado, la temperatura permanece constante: la energía suministrada se utiliza para dilatar y fundir la sustancia. ... · Un líquido puede evaporarse a cualquier temperatura, pero comienza a hervir cuando la presión máxima de vapor iguala la presión externa.
¿Qué les sucede a las moléculas en los cambios de estado?
El calor suministrado o liberado durante el cambio de fase se denomina calor latente molar. Los líquidos y algunos sólidos (moleculares) sufren un proceso continuo de evaporación. La molécula se mantiene en el cuerpo líquido por una fuerza neta de atracción hacia el interior.
¿Cómo se llama el cambio de estado que indica la transformación del hielo en agua?
La fusión es la transición del estado sólido al líquido; el hielo se derrite cuando se deja a temperatura ambiente. Esta transformación tiene lugar con la compra de calor y por tanto es un proceso endotérmico. Durante la fusión de una sustancia pura, la temperatura del sistema permanece constante.
¿Cómo varía el calor latente con la presión?
El calor latente también depende del cambio de fase que se considere y, para una misma sustancia y a la misma temperatura y presión, asume valores numéricos opuestos para cada cambio de estado y para su inverso (dependiendo de si la sustancia absorbe o libera calor).