¿Cuándo el hidrógeno tiene un número de oxidación negativo?
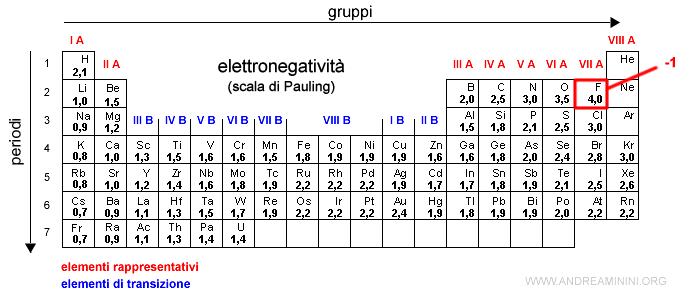
Teniendo en cuenta la definición de número de oxidación, es fácil entender que el hidrógeno asumirá un número de oxidación positivo cuando se une a átomos con electronegatividad más alta que la suya, mientras que asumirá un número de oxidación negativo cuando se une a átomos con menor electronegatividad. electronegatividad
¿Qué número de oxidación tiene el hidrógeno?
2) El hidrógeno tiene un número de oxidación +1 o -1: cuando se une directamente con más metales electropositivos (hidruros), y en los que por lo tanto tiene un número de oxidación -1; +1 cuando se une a no metales (hidrácidos).
¿Por qué el hidrógeno tiene un número de oxidación negativo?
Los átomos de hidrógeno, por otro lado, tienen cero electrones de enlace porque pierden el electrón. Nota. Este es solo un cálculo matemático útil para calcular el número de oxidación. En realidad, los átomos no pierden electrones en los enlaces covalentes porque se comparten.
¿Cuándo H tiene un No negativo?
4) El hidrógeno H siempre no tiene +1, excepto en los hidruros (compuestos binarios con metales) donde no tiene –1. los átomos deben ser cero. En un ion (positivo o negativo) la suma algebraica de los nos debe ser igual a la carga del propio ion.
¿Quién puede tener un número de oxidación negativo?
Otras indicaciones son: los metales tienen solo números de oxidación positivos; los no metales pueden tener números de oxidación positivos o negativos; los elementos del primer grupo (metales alcalinos) siempre tienen no = +1; los elementos del segundo grupo (metales alcalinotérreos) siempre tienen no = +2; elementos de ...
Cómo asignar el número de oxidación
Encuentra 25 preguntas relacionadas
¿Cuál es el número de oxidación del cloro?
El cloro puede asumir los estados de oxidación −1, +1, +3, +5 o +7 correspondientes a los aniones Cl− (cloruro), ClO− (hipoclorito), ClO − 2 (clorito), ClO − 3 (clorato), o ClO − 4 (perclorato).
¿Cómo encontrar el número de oxidación del carbono?
El segundo átomo de carbono, por otro lado, está unido a dos átomos de hidrógeno, un átomo de carbono y un átomo de oxígeno y, por lo tanto, tendrá un número de oxidación igual a (2) (-1) + 0 - 1 = 1.
¿Cómo entiendes quién oxida y quién reduce?
La sustancia que adquiere electrones (O) se reduce y se denomina oxidante. La sustancia que pierde electrones (C) se oxida y se llama agente reductor.
¿Cuándo es el número de oxidación 0?
El número de oxidación de un elemento en una sustancia en su estado elemental siempre es igual a 0. En consecuencia, todos los elementos de la tabla periódica tienen este número de oxidación (aunque a menudo no se informa).
¿Cuándo se oxida un elemento?
Hoy en día el significado del término oxidación es más general que entonces: las oxidaciones se definen como todas aquellas reacciones en las que se produce una pérdida de electrones por parte de una especie química. Estos electrones se transfieren a otra especie química que, al adquirir los electrones, se reduce.
¿Cuál es el número de oxidación del hidrógeno a HF?
El hidrógeno tiene número de oxidación +1, a excepción de los hidruros metálicos (LiH, CuH, ..
¿En qué área de la tabla periódica hay elementos con un número de oxidación que siempre es positivo?
Los metales siempre tienen un número de oxidación positivo. Los Metales Alcalinos, los del Grupo I, nunca tienen '+1'; los Metales Alcalinotérreos, los del Grupo II, nunca tienen '+2'; Los Elementos del Grupo III siempre no tienen '+3'. 8.
¿Cómo se calcula el no?
El número de oxidación de cada átomo se calcula restando la suma de pares de electrones libres y los electrones obtenidos al atraer pares de electrones comunes del número de electrones de valencia.
¿Cómo se calcula el número de oxidación del nitrógeno?
El símbolo ±, como por ejemplo en ± 3, significa que el nitrógeno puede tener tanto el número de oxidación +3 como el número de oxidación -3. Por tanto, en total, los números de oxidación que puede asumir el nitrógeno son 8, es decir: +1, +3, +5, +4, +2, -1, -3, -2.
¿Por qué el número de oxidación 1 se atribuye al oxígeno en el peróxido de hidrógeno?
Para asignar los números de oxidación de H y O en H2O2 es necesario estudiar primero la estructura de la molécula. ... El estado de oxidación -1 del oxígeno en H2O2 es un estado intermedio entre los estados 0 y -2 y, por lo tanto, el peróxido de hidrógeno puede funcionar tanto como agente oxidante como reductor.
¿Por qué el número de oxidación de los halógenos en los compuestos iónicos siempre es 1?
5) Los halógenos (cloro, bromo, yodo) con hidrógeno tienen números de oxidación -1, mientras que con oxígeno tienen números de oxidación positivos porque son menos electronegativos (ejemplo: Cl2O, anhídrido hipocloroso). El flúor siempre tiene número de oxidación - 1, porque es el elemento más electronegativo.
¿Cuál es el número de oxidación del cloro en el ácido clorhídrico?
Por ejemplo, en el ácido clorhídrico H ― Cl, los dos electrones de enlace (uno proveniente del Cl y el otro del H) son atraídos por el cloro, que es el átomo con mayor electronegatividad. El número de oxidación del cloro (Cl) en este compuesto es por tanto -1, el número de oxidación del H es +1.
¿Qué semirreacción representa correctamente una reducción?
Reacciones redox
En esta reacción, el cobre se oxida y la plata se reduce. Oxidación de cobre metálico por iones de plata. Una espiral de cobre se sumerge en una solución de nitrato de plata.
¿Cómo se reconoce un oxidante?
En un sentido más general, los oxidantes son aquellas sustancias que, en una redox, al adquirir electrones disminuyen su número de oxidación. Una sustancia oxidante luego sufre una reducción. Por lo tanto, en una reacción redox siempre hay una sustancia oxidante que se reduce y una sustancia reductora que se oxida.
¿Cómo se reconoce un agente oxidante?
Los agentes oxidantes son sustancias químicas capaces de liberar átomos de oxígeno en una reacción redox. En un sentido más general son aquellas sustancias que, en una redox, al adquirir electrones disminuyen su propio número de oxidación; una sustancia oxidante luego sufre una reacción de reducción.
¿Cómo se atribuye el número de oxidación a los compuestos orgánicos?
Un átomo de carbono alcohólico puede tener un número de oxidación entre -2 y +1 dependiendo del número de grupos alquilo enlazados a él (los electrones del enlace entre el átomo de carbono y el grupo alquilo no están asignados a ninguno de los dos átomos).
¿Cuál es el número atómico del cloro?
cloro Elemento químico del grupo de los halógenos, descubierto por KW Scheele en 1774 y aislado por H. Davy en 1810; símbolo Cl, número atómico 17, peso atómico 35,457; Se conocen dos isótopos estables 3517Cl y 317Cl presentes en la naturaleza en una proporción de aproximadamente 3:1.
¿Cuál es el número de oxidación del cloro en clo4?
El ion perclorato, de fórmula química ClO − 4, es el anión del cloro con estado de oxidación +7. El ion más rico en oxígeno de todos los iones de cloro.