¿Cuál es la diferencia de electronegatividad?
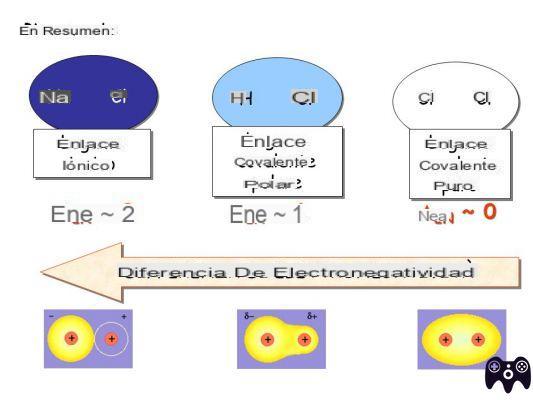
Cuando la diferencia de electronegatividad entre dos átomos es alta, los electrones se transfieren de un átomo a otro, dando como resultado un enlace iónico; cuando la diferencia de electronegatividad entre los átomos es pequeña, los electrones se comparten entre los átomos, lo que da como resultado un enlace covalente.
¿Cómo se hace la diferencia de electronegatividad?
Calcular la diferencia de electronegatividad entre dos átomos.
Resta el valor inferior del superior para encontrar la diferencia. Por ejemplo, si consideramos la molécula de HF, debemos restar la electronegatividad del hidrógeno (2,1) a la del flúor (4,0) y obtenemos: 4,0-2,1 = 1,9.
¿Qué se entiende por electronegatividad de un átomo?
La electronegatividad, símbolo χ, es una propiedad química que describe la tendencia de un átomo a atraer electrones compartidos hacia sí mismo.
¿Qué es una molécula?
molécula, dim. de lat. lunares "topo"]. - Combinación química de dos o más átomos, iguales entre sí (en los elementos) o diferentes (en los compuestos), que pueden existir en estado libre, y que representa la menor cantidad de materia que posee las propiedades características de la sustancia en cuestión.
¿Cómo saber si un enlace es iónico o no?
En principio, es posible distinguir entre dos tipos diferentes de enlaces químicos:- Enlace iónico: Los átomos se unen mediante la transferencia completa de electrones.
- Enlace covalente: los átomos se unen compartiendo electrones.
¿Qué es la ELECTRONEGATIVIDAD?
Encuentra 16 preguntas relacionadas
¿Cómo se distribuyen los electrones en un enlace covalente homopolar?
En un enlace homopolar como el que poseen las moléculas de hidrógeno, oxígeno, nitrógeno, etc., la compartición de los electrones del enlace se produce entre 2 átomos idénticos, por lo que la nube de electrones se distribuye simétricamente alrededor de los dos núcleos.
¿Qué tipo de enlace es el co2?
La molécula de dióxido de carbono es lineal; cada uno de los dos átomos de oxígeno está unido mediante un doble enlace covalente al átomo de carbono. El ángulo de enlace neutraliza los dos momentos dipolares opuestos de cada doble enlace C = O, por lo que la molécula es globalmente apolar.
¿Cómo se forma una molécula?
Está formado por la agregación de átomos que son iguales o diferentes entre sí. De acuerdo con los enlaces entre los diversos átomos, los diferentes elementos se "componen". Veamos dos ejemplos básicos: el hierro es un elemento formado por átomos iguales, mientras que el agua, cuya fórmula es H2O, está formada por dos átomos de hidrógeno y uno de oxígeno.
¿Cuál es la diferencia entre un átomo y una molécula?
Todos los materiales que existen están formados por partículas muy pequeñas en continuo e incesante movimiento, que pueden ser átomos o moléculas. Los átomos son las partículas individuales más simples, mientras que las moléculas están formadas por dos o más átomos, iguales o diferentes, unidos entre sí.
¿Qué son las moléculas de la escuela primaria?
¿Qué son las moléculas de la escuela primaria? Una molécula es el agregado más pequeño de átomos que caracteriza a una sustancia y se puede representar con una fórmula. En los elementos las moléculas están formadas por átomos de la misma especie, en los compuestos en cambio, están formadas por átomos de diferente especie.
¿Qué es la electronegatividad y cómo varía en la tabla periódica?
En la escala de Pauling los valores de electronegatividad para H y Cl son: 2,2 y 3,16. Como este valor es superior a 0,5 podemos decir que el enlace Cl-H es siempre un enlace polar.
¿Cómo saber si un elemento es más electronegativo?
Como puede verse, la electronegatividad aumenta en un grupo de abajo hacia arriba y en un período de izquierda a derecha: en consecuencia, los elementos más electronegativos se encuentran en la esquina superior derecha mientras que los menos electronegativos se encuentran en el lado opuesto, en el esquina inferior izquierda.
¿Cuándo es un elemento más electronegativo?
La electronegatividad es la capacidad de un átomo para atraer hacia sí los electrones de enlace. Los elementos más electronegativos pertenecen al grupo VII subgrupo A (VIIA) y el flúor (F) es el elemento más electronegativo, su electronegatividad según Pauling es igual a 4.
¿Cómo sabes cuántos enlaces hace un elemento?
Los átomos se unen compartiendo electrones. En un enlace típico, se comparten dos electrones, uno para cada uno de los átomos involucrados. El carbono tiene cuatro electrones tan compartibles, por lo que tiende a formar cuatro enlaces con otros átomos.
¿Cuáles son los tres tipos de enlaces químicos?
Tipos de enlace químico- Antijuego.
- Enlace covalente.
- Vínculo de coordinación.
- Enlace iónico.
- Enlace de hidrógeno.
- Enlace metálico.
¿Cuáles son los lazos más fuertes?
El enlace covalente es el enlace químico más fuerte y existen dos tipos de enlace covalente: 1 - el enlace covalente puro; 2- el enlace covalente polar. Un enlace covalente se llama "puro" cuando se forma entre átomos con el mismo valor de electronegatividad, o valores muy cercanos.
¿Cómo se escriben los átomos?
Para evitar confusiones, cabe señalar que cada elemento está marcado con un símbolo. ... Cuando reportamos el símbolo de un elemento indicamos un átomo de ese elemento: por ejemplo, si escribimos H nos referimos a un átomo de hidrógeno, si escribimos Na indicamos un átomo de sodio, y así sucesivamente.
¿Cuál es la diferencia entre un átomo y un ion?
Los átomos son eléctricamente neutros ya que contienen el mismo número de protones y electrones. Sin embargo, los átomos de muchos elementos pueden perder o adquirir electrones. El resultado es la formación de una especie que tiene carga eléctrica positiva o negativa, que se denomina ion.
¿Cómo se forman las moléculas?
Todas las moléculas están formadas por átomos que se mantienen unidos por un enlace químico, y el peso de la molécula se determina en una unidad de medida llamada unidad de masa atómica (uma).
¿Cómo entender la estructura de Lewis?
A cada elemento le asignamos sus electrones, que dibujamos como puntos que rodean al átomo arriba, abajo, a la izquierda y a la derecha, como si estuvieran en lo alto de una hipotética cruz. Si hay más de cuatro electrones para arreglar, debemos comenzar a emparejarlos para formar dobletes.
¿Cómo se determina la estructura de Lewis?
Cómo escribir las estructuras de Lewis de los elementos
Luis. Según este método, los ocho electrones de la capa más externa de un átomo se representan como puntos o pares de puntos dibujados en los cuatro lados del símbolo químico del elemento.
¿Qué tipo de enlace es h2s?
Hay dos enlaces covalentes polarizados en la molécula de sulfuro de hidrógeno. La carga negativa parcial se encuentra en el átomo de azufre más electronegativo.
¿Qué tipo de enlace es el HCl?
Enlace covalente polar
Hemos visto que en el enlace covalente puro, los electrones se comparten entre átomos del mismo elemento. ... Considere, por ejemplo, la molécula de ácido clorhídrico (HCl) en la que H y Cl comparten un par de electrones.
¿Cuándo es un enlace apolar?
Hablamos de enlace covalente puro si se da entre átomos iguales. Si se produce entre átomos con una diferencia de electronegatividad entre cero y 0,4, se denomina covalente homopolar o apolar. ... Un enlace covalente homopolar ocurre cuando la diferencia de electronegatividad entre dos átomos es menor o igual a 0,4.