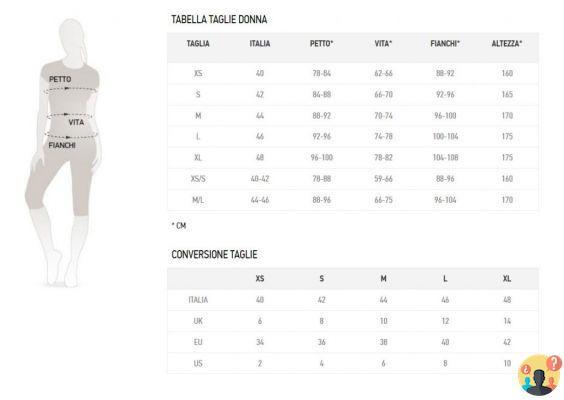
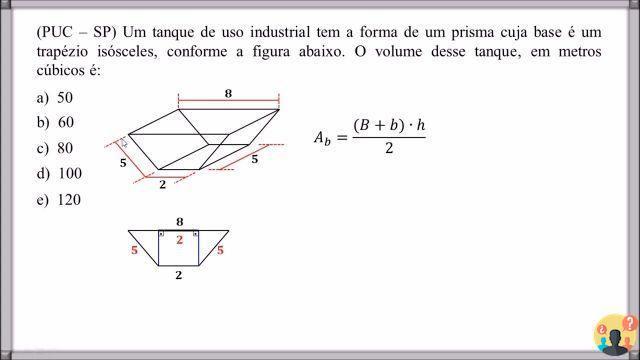
¿Cómo están ubicados los muelles?
El número de moles (n) se calcula dividiendo la masa dada (m), expresada en gramos, por la masa de un mol de la sustancia considerada, generalmente indicada como peso molar (PM) expresado en g/mol.
¿Cómo se pasa de moles a gramos?
El número de moles de un determinado compuesto químico se puede calcular dividiendo el número de gramos por la masa molecular. La fórmula es la siguiente: moles = gramos de compuesto químico / masa molecular del compuesto químico.
¿Cómo se encuentran los gramos de una disolución?
Para calcular la masa en gramos de una sustancia conociendo el número de moles, multiplique el número de moles por el valor de la masa molar. La masa molar de un compuesto es la suma de todas las masas atómicas de los elementos que forman la molécula y su unidad de medida es g/mol.
¿Cuántos moles de agua hay en un litro de agua?
5: la respuesta. El numero de moles de agua es 1000g: 18g = 55,6. El número de moles de sustancia se calcula dividiendo la masa en gramos por la masa de un mol que corresponde al peso molecular expresado en gramos. Como la densidad del agua es de 1 Kg/L, un litro de agua tiene la masa de 1 Kg = 1000 g.
¿Cómo encontrar lunares con volumen?
En la fórmula tenemos: M = n/V de esta fórmula obtenemos las fórmulas inversas: n = M * V y V = n/M que permiten realizar cálculos de diferente tipo.
Mole y número de Avogadro
Encuentra 20 preguntas relacionadas
¿Cómo encontrar el número de moles con el número de Avogadro?
El concepto de mol se refiere por un lado a la masa, más precisamente a la masa molar, y por otro lado al número de moléculas que contiene, que es igual al número de Avogadro, NA, y vale 6,022 × 1023 moléculas/ mol.
¿Cómo encontrar la molaridad sin volumen?
Divide el número de moles por el número de litros.
Ahora que tienes la cantidad de litros, puedes dividir la cantidad de moles de soluto por este valor para encontrar la molaridad de la solución.
¿Cuántos moles hay en 36 g de agua?
Cada molécula de agua está formada por dos átomos de hidrógeno (PA = 1,008 u) y un átomo de oxígeno (MW = 16,0 u). Luego calculamos el número de moles de agua dividiendo la masa en gramos (= 36 g) por el valor de su masa molar. Entonces, en 36,0 g de agua hay 2,0 moles de agua.
¿Cuántos moles de agua hay en un litro a 4 grados?
En conclusión: en un litro de agua hay 55,56 mol de agua.
¿Cuántos moles de hidrógeno hay en una molécula de agua?
De hecho, si en un mol de agua hay 6,022 · 1023 moléculas de agua y en cada molécula de agua hay dos átomos de hidrógeno, es bastante intuitivo decir que en 6,022 · 1023 moléculas de agua hay el doble de átomos de hidrógeno , es decir: 2 6,022 1023 = 1,204 1024 átomos de hidrógeno.
¿Cómo encontrar los gramos que tienen el volumen?
- En un litro hay 700 ml de etanol.
- La masa se debe calcular: g =% v (volumen) * d = 0.70 * 1000ml * 0.789g/m.
- Pasamos al número de moles: g/MW = 552.3g/46.02g/mol = 12.0mol.
- La molaridad se obtiene: M = n° moles / l = 12.0 mol / 1l = 12M.
¿Cómo saber el número de átomos de un elemento?
Sustituyendo los datos tendremos: n = m/PM = 0,37 mol. Ahora podemos aplicar el número de Avogadro en la fórmula: nx NA = (0,37 mol) x (6,023 x 10^23 mol^-1) = 2,23 x 10^23 átomos. Este resultado define el número de átomos contenidos dentro de una unidad molecular.
¿Cómo encontrar gramos a partir de la masa molar?
De la definición sabemos que la masa molar de una sustancia es la masa en gramos de un mol de la sustancia bajo consideración. de partículas contenidas en 1 mol. En definitiva, la masa molar de una sustancia se obtiene multiplicando el valor del peso molecular (o peso atómico) por 1 g/mol. Con eso es todo!
¿Cómo se pasa de moles a átomos?
De gramos a numero de atomos- Para este cálculo es necesario saber que en un mol de cualquier sustancia pura hay un número de Avogadro (6,022 · 1023) de partículas (en nuestro caso átomos).
- 1 mol: 6,022 · 1023 atomio = 4,0 mol: X.
- X = (6,022 · 1023 atomio · 4,0 mol) / 1 mol = 2,41 · 1024 atomio.
¿Cómo pasar de gramos por litro a moles por litro?
De gramos a molaridad- nsoluto son los moles de soluto disueltos en la solución;
- Vsolución es el volumen de la solución en litros. Para determinar el número de moles de soluto, se debe aplicar la siguiente fórmula: ...
- Mm = masa molar del soluto. ...
- Mm (NaOH) = 23 + 16 + 1 = 40 g/mol. ...
- n = g / Mm = 20 / 40 = 0,5 mol.
¿Cuántos gramos de H2SO4 contiene?
[C] La respuesta correcta fue 49 g. En una solución acuosa de ácido sulfúrico 2M contiene 2 moles de H2SO4 por litro, en 250 ml habrá 0,5 moles. Como cada mol de ácido sulfúrico pesa 98 g, divídelo entre dos.
¿Cómo se pasa de litros a moles?
Para conocer la concentración molar, divida la cantidad de moles que acaba de obtener por 20 litros: 0,6 / 20L moles = 0,03 mol / L.
¿Cuántos litros contiene un mol?
condiciones de temperatura y presión, un mol de cualquier gas ocupa el mismo volumen. (1 atm y 0°C) es igual a 22,4 l.
¿Cuántos kg son 1 litro?
Pero, en general, se puede decir que 1 litro de agua equivale a 1 kg. Además, para una conversión precisa, se puede utilizar el valor del peso específico del agua (que representa la relación entre la masa y el volumen de una sustancia): es igual a 997 Kg/m3.
¿Cómo calcular la cantidad de agua?
Obtuvimos así la masa en gramos de 100 ml de agua. Calculamos la masa molar del agua multiplicando el peso molecular del agua por 1 g/mol. La fórmula química del agua es H2O, por lo que su peso molecular PM (H2O) se obtiene sumando los pesos atómicos de los átomos individuales que componen la molécula de agua.
¿Qué es la Molalita?
La concentración molal (símbolo: b) es una unidad de medida de la concentración de una especie química en una solución. La molalidad se usa menos que la molaridad, pero esta última, al estar referida al volumen, toma un valor que cambia con la temperatura, lo que no sucede, sin embargo, con la molalidad.
¿Cuánto pesa medio mol de agua?
La masa molar del agua es 18,016 g/molH₂O. En el caso del metano (CH4), cuya masa molecular es 16,04, medio mol (por tanto, la mitad del valor numérico de la constante de Avogadro de las moléculas) corresponde a 8,02 gramos.
¿Cómo calcular M en química?
La fórmula para calcular la concentración molar de un soluto es dividir el número de moles del soluto por el volumen de la solución.
¿Para qué sirve la Molaridad?
La molaridad (M) de una solución, también conocida como concentración molar, expresa el número de moles (n) de soluto contenidos en un litro de solución. Operacionalmente, la molaridad viene dada por la relación entre el número de moles de soluto y el volumen en litros de la solución en la que están disueltos.
Come faccio a calcolare il volumen?
La fórmula es: Volumen = largo * profundidad * altura o V = lph. Encuentra la longitud del sólido.