¿A qué corresponde el número de oxidación de un elemento?
El número de oxidación se define como la carga, real (para enlaces iónicos) o formal (para enlaces covalentes), que adquiere un átomo cuando los electrones de enlace se asignan convencionalmente al átomo más electronegativo. ... Cada elemento químico puede tener más de un número de oxidación.
¿Cómo puedo saber el número de oxidación de un elemento de un compuesto ternario?
Por tanto, para calcular los números de oxidación de los elementos de un compuesto es necesario establecer cuál de ellos es el más electronegativo y atribuirle todos los electrones de enlace. Después de esta atribución ficticia vemos la carga que asumen los átomos.
¿Dónde está el número de oxidación en la tabla periódica?
El número de oxidación de un elemento en una sustancia en su estado elemental siempre es igual a 0. En consecuencia, todos los elementos de la tabla periódica tienen este número de oxidación (aunque a menudo no se informa).
¿Cómo se elige el número de oxidación?
En un compuesto, la suma de todos los números de oxidación debe ser igual a cero. Si hay un ion que tiene dos átomos, por ejemplo, la suma de los números de oxidación debe ser igual a la carga del ion.
¿Cómo funcionan los números de oxidación?
1) compuestos iónicos en los que el número de oxidación corresponde a la carga del ion, es decir, el número de electrones perdidos o ganados por el elemento; 2) compuestos con enlaces covalentes en los que el número de oxidación de los elementos se obtiene asignando los electrones de enlace al átomo más electronegativo.
NÚMERO DE OXIDACIÓN - ¿CÓMO SE ASIGNA - QUÍMICA PARA PRUEBAS Y PRUEBAS DE MEDICINA?
Encuentra 43 preguntas relacionadas
¿Cómo se calcula el no?
El número de oxidación de cada átomo se calcula restando la suma de pares de electrones libres y los electrones obtenidos al atraer pares de electrones comunes del número de electrones de valencia.
¿En qué área de la tabla periódica hay elementos con un número de oxidación que siempre es positivo?
Los metales siempre tienen un número de oxidación positivo. Los Metales Alcalinos, los del Grupo I, nunca tienen '+1'; los Metales Alcalinotérreos, los del Grupo II, nunca tienen '+2'; Los Elementos del Grupo III siempre no tienen '+3'. 8.
¿Cómo se asignan los números de oxidación de Zanichelli?
¿Cómo se asignan los números de oxidación en una fórmula? En un compuesto, los números de oxidación se asignan atribuyendo los electrones de enlace al átomo más electronegativo.
¿Cómo calcular el número de oxidación de los iones poliatómicos?
los iones monoatómicos tienen un número de oxidación igual a la carga del ion (por ejemplo, el ion cobre Cu2+ no tiene +2); en un ion poliatómico, la suma algebraica de los números de oxidación de todos los átomos es igual a la carga del ion (por ejemplo, SO no tiene = −2).
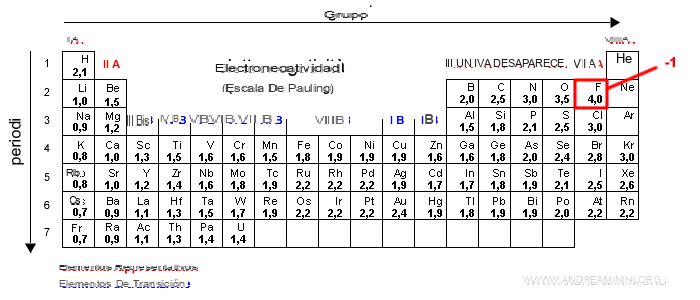
¿Dónde está la electronegatividad en la tabla periódica?
Como puede verse, la electronegatividad aumenta en un grupo de abajo hacia arriba y en un período de izquierda a derecha: en consecuencia, los elementos más electronegativos se encuentran en la esquina superior derecha mientras que los menos electronegativos se encuentran en el lado opuesto, en el esquina inferior izquierda.
¿Cómo se calcula el número de oxidación del nitrógeno?
El símbolo ±, como por ejemplo en ± 3, significa que el nitrógeno puede tener tanto el número de oxidación +3 como el número de oxidación -3. Por tanto, en total, los números de oxidación que puede asumir el nitrógeno son 8, es decir: +1, +3, +5, +4, +2, -1, -3, -2.
¿Cómo se forma el óxido de aluminio?
Disolver la película de aluminio en ácido clorhídrico para obtener cloruro de aluminio que luego se hace reaccionar con bicarbonato de sodio o carbonato de sodio. Posteriormente, es suficiente filtrar todo para obtener hidróxido de aluminio, luego se obtiene óxido de aluminio calentando el hidróxido a 500°C.
¿Cuál es la fórmula que corresponde a un compuesto ternario?
Por ejemplo, el compuesto HClO3 es un compuesto ternario porque está formado por H (hidrógeno) Cl (cloro) y O (oxígeno), H2SO4 es un compuesto ternario porque está formado por H (hidrógeno) Azufre (S) y O (oxígeno).
¿Cómo conseguir sal ternaria?
Las sales ternarias (o sales de oxiácidos) se componen de tres elementos: un metal, un no metal y oxígeno. Se obtienen reemplazando el hidrógeno por un no metal en un oxiácido. En la fórmula escribimos primero el metal, luego el no metal y, por último, el oxígeno.
¿Cómo entiendes quién oxida y quién reduce?
La sustancia que adquiere electrones (O) se reduce y se denomina oxidante. La sustancia que pierde electrones (C) se oxida y se llama agente reductor.
¿Cuándo el número de oxidación es negativo?
Este es el caso de las sustancias simples, tales como: H2, O2, F2 N2, Cl2. En otros casos, el número de oxidación de un átomo es positivo si se liberan los electrones, mientras que es negativo si se compran.
¿Qué cambio en el número de oxidación representa una oxidación?
Como se anticipó, el número de oxidación (no) representa la carga formal que se le puede atribuir a un elemento en un compuesto, asumiendo que los enlaces son de tipo iónico, para asignar los electrones de enlace al elemento más electronegativo.
¿Cuándo el hidrógeno tiene un número de oxidación negativo?
Teniendo en cuenta la definición de número de oxidación, es fácil entender que el hidrógeno asumirá un número de oxidación positivo cuando se une a átomos con electronegatividad más alta que la suya, mientras que asumirá un número de oxidación negativo cuando se une a átomos con menor electronegatividad. electronegatividad
¿Cuál es la diferencia entre número de oxidación y valencia?
El número de oxidación, que en el caso de los iones corresponde a la carga iónica, puede asumir, a diferencia de la valencia, valores positivos y negativos, pero también el valor cero. Algunos elementos pueden tener dos o más números de oxidación y en estos casos la nomenclatura sigue criterios adecuados para distinguirlos.
¿Cuáles son los elementos más electronegativos de la tabla periódica?
La electronegatividad es la capacidad de un átomo para atraer hacia sí los electrones de enlace. Los elementos más electronegativos pertenecen al grupo VII subgrupo A (VIIA) y el flúor (F) es el elemento más electronegativo, su electronegatividad según Pauling es igual a 4.
¿Cuántos números de oxidación tiene el cobre?
Los dos estados de oxidación más comunes del cobre son +1 (ión cuproso, Cu+) y +2 (ión cúprico, Cu2+). Dos ejemplos son su óxido de cobre (I) (Cu2O) y el óxido de cobre (II) (CuO).
¿Cuál es el número de oxidación del Cl?
El cloro puede asumir los estados de oxidación −1, +1, +3, +5 o +7 correspondientes a los aniones Cl− (cloruro), ClO− (hipoclorito), ClO − 2 (clorito), ClO − 3 (clorato), o ClO − 4 (perclorato).